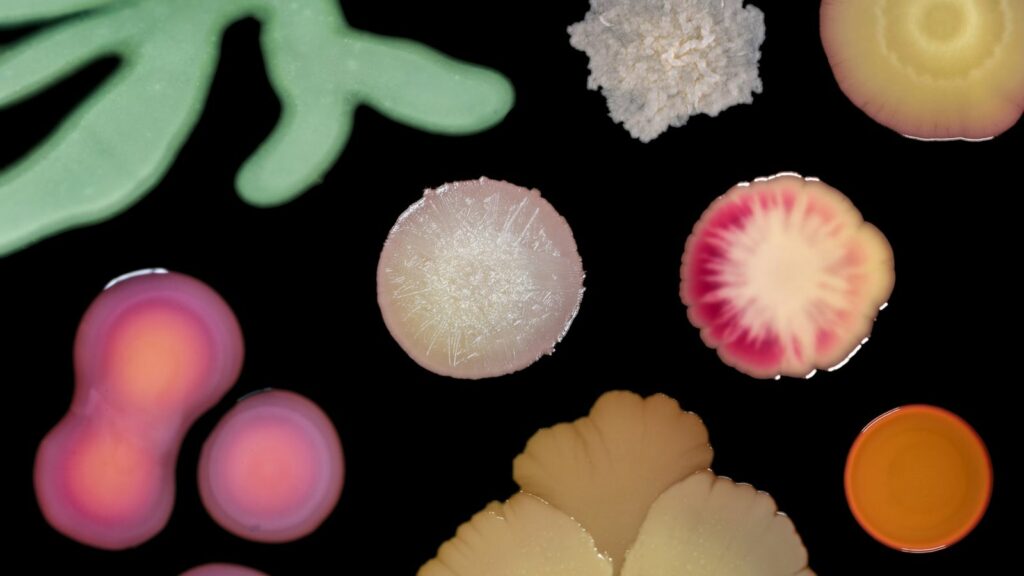
FOTO DE COMPOSITE BY SCOTT CHIMILESKI, MICROBEPHOTOGRAPHY.COM, AND ROBERTO KOLTER, HARVARD MEDICAL SCHOOL
Especialistas em saúde pública temem que o uso indevido e excessivo de antibióticos durante a pandemia possa piorar outra crise já existente: a resistência a antibióticos, na qual patógenos como bactérias e fungos evoluem e conseguem escapar da ação dos medicamentos poderosos criados para destruí-los.
Mais de 750 mil pessoas morrem anualmente de infecções resistentes a antibióticos e esse número deve chegar a 10 milhões até 2050. Somente nos Estados Unidos, micróbios resistentes a antibióticos causam mais de 2,8 milhões de infecções e mais de 35 mil mortes todos os anos.
Agora, o uso excessivo de antibióticos durante a pandemia de covid-19 pode estar piorando o problema. Nos primeiros meses da pandemia, quando os pacientes com covid-19 apresentavam tosse, febre, falta de ar e as radiografias de tórax revelavam manchas brancas — inflamação pulmonar semelhante à causada por uma pneumonia bacteriana — muitos receberam a prescrição de antibióticos. Nos Estados Unidos, por exemplo, mais da metade dos quase cinco mil pacientes hospitalizados entre fevereiro e julho de 2020 receberam prescrição de pelo menos um antibiótico nas primeiras 48 horas de internação.
“Quando estão lidando com a incerteza, os médicos preferem prescrever, o que não é necessariamente a coisa certa a ser feita”, explica Jacqueline Bork, médica de doenças infecciosas do Centro Médico da Universidade de Maryland.
Os antibióticos matam apenas bactérias e não vírus como o SARS-CoV-2, que causa a covid-19. Contudo, pneumonias podem ser causadas por fungos, bactérias ou vírus, e descobrir o patógeno responsável pode levar pelo menos 48 horas e, em alguns casos, são necessários procedimentos invasivos para confirmar a causa da infecção. Às vezes, os exames não identificam o culpado. “Muitos de nós provavelmente estavam prescrevendo antibióticos em excesso. Mas sem o conhecimento necessário sobre aquilo que estávamos lidando, fizemos o melhor que pudemos na época”, afirma Bork.
Alguns médicos também estavam preocupados que uma infecção fúngica ou bacteriana pudesse ocorrer durante ou após a covid-19, semelhante ao observado na gripe e em outras doenças virais. “No começo, o número de pessoas admitidas com pneumonia era tão alto que não conseguíamos realizar exames para saber se era infecção viral ou bacteriana”, explica Bork.
Conforme ela e outros médicos em todo o mundo descobriram que infecções fúngicas e bacterianas concomitantes ocorriam em menos de 20% dos pacientes com covid-19, alguns reduziram o uso de antibióticos. Mas para os pacientes que estavam gravemente doentes e ficavam internados por mais tempo, os antibióticos eram necessários, pois muitas vezes esses pacientes ficavam intubados e tinham cateteres que poderiam causar infecções bacterianas e até mesmo sepse.
Ainda assim, em muitas partes do mundo, os médicos continuaram prescrevendo antibióticos a pacientes com covid-19 que podem não precisar desses medicamentos. Quando ficou mais difícil consultar um médico, os pacientes recorreram à automedicação com antibióticos, às vezes até mesmo como medida preventiva. O custo e a falta de acesso a exames de diagnóstico para confirmar a origem bacteriana da infecção e, portanto, a necessidade de antibióticos, atitudes do tipo “na dúvida, é melhor tomar” e a falta de conhecimento sobre as descobertas científicas mais recentes podem ter contribuído para o uso excessivo e indevido de antibióticos durante a pandemia.
Como se desenvolve a resistência antimicrobiana
Na natureza, fungos e bactérias do solo produzem substâncias químicas chamadas antibióticos que matam ou inibem o crescimento de outras bactérias que competem pelos mesmos recursos limitados. Com o tempo, os alvos se adaptam, desenvolvendo resistência contra tal mecanismo. Eles fazem isso produzindo proteínas chamadas enzimas que inativam o antibiótico, drenam o medicamento das células bacterianas, restringem sua entrada ou contornam seus efeitos. Às vezes, outras espécies bacterianas que não eram o alvo original dos antibióticos também podem desenvolver defesas, adquirindo genes importantes de bactérias resistentes que estão ao seu redor, por meio de um processo chamado transferência horizontal de genes.
Esses antibióticos naturais foram utilizados pelos cientistas como base para desenvolver medicamentos comerciais que combatem infecções bacterianas em humanos e animais. Mas é provável que algumas dessas bactérias responsáveis pelas infecções, encontradas na água e no solo, já tenham adquirido genes que conferem resistência.
Inicialmente, as bactérias resistentes representam uma pequena parcela da população bacteriana encontrada nos hospedeiros, mas isso muda com o aumento do uso de antibióticos. O medicamento destrói as bactérias suscetíveis, eliminando assim a competição e permitindo que as bactérias resistentes se reproduzam e prosperem rapidamente. Além disso, administrar doses incorretas de antibióticos ou usá-los de forma inadequada, por exemplo, para uma doença diagnosticada errada, pode destruir as bactérias boas do nosso organismo e estimular o estabelecimento das chamadas superbactérias resistentes a diversos antibióticos.
Essas bactérias resistentes a medicamentos podem se propagar em hospitais, comunidades, e fazendas de criação de gado e aves por meio do esgoto, água, superfícies e alimentos contaminados — ou por contato direto. Com mais pessoas infectadas por superbactérias e os antibióticos atuais se tornando cada vez mais ineficazes, as consequências podem incluir hospitalizações prolongadas, custos médicos mais altos e mais mortes. Isso é particularmente preocupante para países de baixa e média renda que são desproporcionalmente impactados devido ao acesso limitado a água potável e saneamento, falta de assistência médica de qualidade e acesso a antibióticos sem necessidade de receita médica, o que pode incentivar a automedicação nos casos em que a consulta médica tem um alto custo.
Como a covid-19 pode exacerbar infecções resistentes a diversos medicamentos
Em uma pesquisa global realizada pela Organização Mundial da Saúde no final de 2020, 35 dos 56 países relataram um aumento na prescrição de antibióticos durante a pandemia. Em um país, os médicos prescreveram antibióticos em quase todos os casos de covid-19 e outro país relatou automedicação desenfreada com esses medicamentos.
Médicos prescreveram antibióticos para pacientes hospitalizados com covid-19, incluindo azitromicina, doxiciclina, fluoroquinolonas, cefalosporinas e carbapenêmicos. Os profissionais costumam prescrever antibióticos de amplo espectro que destroem diversos tipos de bactérias, incluindo as benéficas, embora diversos estudos tenham sugerido que as taxas de infecção bacteriana ou fúngica concomitante ou infecção secundária sejam inferiores a 20% entre os pacientes com covid-19. Pacientes ambulatoriais, muitas vezes com sintomas leves de covid-19, também receberam prescrição preventiva de antibióticos, como azitromicina e doxiciclina.
No início da pandemia, alguns estudos recomendaram o uso de azitromicina e doxiciclina devido às suas possíveis propriedades antivirais e anti-inflamatórias que poderiam ajudar a controlar o sistema imunológico hiperativo de um paciente com covid-19 quando ele começa a destruir suas próprias células. Mas trabalhos mais recentes não sugeriram benefícios reais.
“Muitos pacientes com covid-19 me procuram para uma segunda opinião e ainda vejo azitromicina em suas prescrições”, diz Lancelot Pinto, pneumologista do P.D. Hospital Hinduja em Mumbai, na Índia. “Talvez a justificativa seja a possibilidade de uma infecção bacteriana e, portanto, é melhor estar protegido, mas acredito que muitos médicos [na Índia] não se importam se é um vírus ou não quando se trata de prescrever antibióticos.”
Em outros casos, os médicos se sentiram compelidos a prescrever azitromicina em zonas rurais, por exemplo, que não têm acesso a exames de diagnóstico, como radiografia, para confirmar pneumonia, muito menos descobrir se a infecção é de origem bacteriana, fúngica ou viral.
“Quando as pessoas não estão tão confiantes, elas costumam achar que é melhor prevenir do que remediar”, diz Rumina Hasan, patologista da Universidade Aga Khan em Karachi, no Paquistão. Ela aponta que alguns usos inadequados e excessivos de antibióticos durante a pandemia também foram impulsionados por médicos desinformados ou incapazes de acompanhar as informações atualizadas sobre a covid-19. “E uma vez que uma tendência foi estabelecida [de usar certos medicamentos contra uma doença], é muito difícil mudá-la”, explica Hasan.
Embora os antibióticos possam salvar vidas quando usados adequadamente, especialistas em saúde global suspeitam que seu uso generalizado e indiscriminado durante a pandemia possa ter criado o cenário ideal para a seleção de bactérias resistentes.
Daqui para frente
Podemos não ver o aumento das superbactérias e seus impactos ainda, mas “o estrago está feito”, diz Pilar Ramon-Pardo, consultora regional de resistência antimicrobiana da Organização Pan-Americana da Saúde. O Sistema Global de Vigilância de Uso e Resistência Antimicrobiana, lançado pela OMS em 2015, foi prejudicado durante a pandemia pela redução do número de equipes médicas em todo o mundo que trabalha na coleta de amostras e registro de micróbios resistentes a medicamentos.
Com todos os recursos desviados para o combate à covid-19, a crise orçamentária e a fadiga mental também estão em jogo. “As pessoas não estão interessadas em mais uma crise de saúde pública”, diz Muhammad Zaman, professor de engenharia biomédica da Universidade de Boston. “Algo vai sair prejudicado.”
Mas se as infecções resistentes a antibióticos aumentarem no mundo pós-pandemia, será que novos antibióticos serão desenvolvidos para combatê-las? Provavelmente não tantos, diz Zaman. Os tratamentos com antibióticos raramente excedem 14 dias e não trazem lucros confortáveis às farmacêuticas, como terapias para doenças crônicas, como câncer e diabetes. Os novos medicamentos provavelmente também serão atingidos pela questão da resistência com bastante rapidez, tornando os investimentos em inovação menos lucrativos.
No entanto, em 2013, os Institutos Nacionais de Saúde lançaram um programa de resistência antibacteriana para conduzir e financiar pesquisas destinadas a testar novos medicamentos e ferramentas de diagnóstico, bem como otimizar o uso dos antibióticos existentes. Para especialistas em saúde global, a solução está em aumentar a prevenção e o controle de infecções. As vacinas atualmente em desenvolvimento contra patógenos resistentes a medicamentos também podem ser promissoras.
“Mas a ideia de que esse problema seja puramente científico é incompleta e imprecisa”, comenta Zaman. “Temos que pensar em economia, acesso e comportamento humano.”
Fonte: National Geographic Brasil